| Kation Na+
je ionizován a reakce se neúčastní |
| Hydrogenfosforečnan v první reakci vystupuje jako
kyselina: |
První
reakce:
HPO4-2
+H2O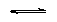 PO4-3
+ H3O+ PO4-3
+ H3O+ |
| Některé
z H3O+ vzniklé v první reakci
vstupují do reakce s HPO4-2. |
Druhá reakce:
HPO4-2
+H3O+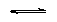 H2PO4- + H2O H2PO4- + H2O |
| Druhá
disociační konstanta pro trojsytnou kyselinu H3PO4 (odpovídá druhé reakci zprava!!): |
| |
|
[HPO4-2].[H3O+] |
| KH2PO4- |
= |
|
| |
|
[H2PO4-] |
|
| Třetí
disociační konstanta pro trojsytnou kyselinu H3PO4 (odpovídá první reakci): |
| |
|
[PO4-3].[H3O+] |
| KHPO4-2 |
= |
|
| |
|
[HPO4-2] |
|
| Všechny sloučeniny v obou reakcích jsou ve stavu rovnovážném. Upozorňuji, že rovnovážná koncentrace H3O+
v obou reakcích je totožná. V první
reakci vzniklo H3O+
více, některé z H3O+ zanikly v reakci
druhé. |
[H3O+(rovnovážná)] =
= [H3O+(vzniklá)] - [H3O+(zaniklá)] |
| V první reakci vzniklo
PO4-3
stejně jako H3O+,
pro PO4-3 se zároveň jedná o koncentraci
rovnovážnou, neboť se v druhé reakci
nevyskytuje a tudíž nemůže ubývat jako [H3O+]. |
[H3O+(vzniklá)]=
= [PO4-3(vzniklá)] =
[PO4-3(rovnovážná)] |
| Třetí
disociační konstantu lze tedy upravit: |
| |
|
[H3O+(vzniklá)].[H3O+(rovnovážná)] |
| KHPO4-2 |
= |
|
| |
|
[HPO4-2] |
|
| Z toho plyne, že koncentrace vzniklé
H3O+
je: |
| |
|
KHPO4-2.[HPO4-2] |
| [H3O+(vzniklá)] |
= |
|
| |
|
[H3O+(rovnovážná)] |
|
| V druhé reakci vznikala
H2PO4-.
každá molekula H2PO4-
vznikla zánikem
H3O+,
znamená, že koncentrace vzniklé
H2PO4-
se rovná koncenraci zániklé
H3O+.H2PO4-
vzniklo tolik, až nastala rovnovážná koncentrace: |
[H2PO4-(vzniklá)] =[H3O+(zaniklá)]
[H2PO4-(vzniklá)] = [H2PO4-(rovnovážná)]
[H2PO4-(rovnovážná)] = [H3O+(zaniklá)] |
| Druhou
disociační konstantu lze tedy upravit: |
| |
|
[HPO4-2].[H3O+(rovnovážná)] |
| KH2PO4- |
= |
|
| |
|
[H3O+(zaniklá)] |
|
| Z toho plyne, že koncentrace zaniklé
H3O+
je: |
| |
|
[HPO4-2].[H3O+(rovnovážná)] |
| [H3O+(zaniklá)] |
= |
|
| |
|
KH2PO4- |
|
| Pro rovnovážnou
koncentraci [H3O+] jak již výše
uvedeno platí: |
| [H3O+(rovnovážná)] =
[H3O+(vzniklá)] - [H3O+(zaniklá)] |
| Po dosazení pak: |
| |
|
KHPO4-2.[HPO4-2] |
|
[HPO4-2].[H3O+(rovnovážná)] |
| [H3O+(rovnovážná)] |
= |
|
- |
|
| |
|
[H3O+(rovnovážná)] |
|
KH2PO4- |
|
Po
úpravě platí:
[H3O+].[H3O+].KH2PO4- = KHPO4-2.[HPO4-2].KH2PO4-
- [HPO4-2].[H3O+].[H3O+] |
| [H3O+].[H3O+]. ( KH2PO4- +[HPO4-2] ) = KHPO4-2.[HPO4-2].KH2PO4- |
| [H3O+] |
= |
( |
| KHPO4-2.[HPO4-2].KH2PO4- |
|
| KH2PO4- + [HPO4-2] |
|
) |
1/2 |
|
| Kyselina uhličitá je slabá KH2PO4-
= 6,23.10-8
, proto lze KH2PO4-
proti rovnovážné
koncentraci [HPO4-2] ve
jmenovateli zanedbat {analytická koncentrace [HPO4-2] = rovnovážná koncentrace cHPO4-2 viz.sůl
slabé kyseliny a silné zásady}. |
| Pak po úpravě platí: |
| [H3O+] |
= |
( |
KHPO4-2.[HPO4-2].KH2PO4-
|
|
[HPO4-2] |
|
) |
1/2 |
|
[H3O+] =(KHPO4-2.KH2PO4-)1/2 |
Zde je po
zlogaritmování výsledek:
| pH =1/2 (pKHPO4-2 +pKH2PO4-) |
!!!Všimněte si ,
že v něm nezávisí výsledek vůbec na koncentraci
roztoku!!!
Zde klik na výpočty pH amfolytů
různých koncentrací:
a) od kyseliny slabé -
uhličité b) od kyseliny
téměř silné - siřičité c) od kyseliny silné - sírové
Zde
klik na kompletní odvození u hydrogenuhličitanu,
Zde
klik na kompletní odvození u hydrogefosforečnanu,
Zde
klik na kompletní odvození u dihydrogenfosforečnanu
|