kyselina
trihydrogenfosforečná
|
| Pro trojsytnou
kyselinu H3PO4 platí 3 disociační
konstanty |
První disociační konstanta pro
rovnici:
H3PO4 + H2O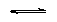 H2PO4- + H3O+ H2PO4- + H3O+ |
| |
|
[H2PO4-].[H3O+] |
| KH3PO4 |
= |
|
| |
|
[H3PO4 ] |
|
Druhá disociační konstanta pro
rovnici:
H2PO4- + H2O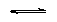 HPO4-2 + H3O+ HPO4-2 + H3O+ |
| |
|
[HPO4-2].[H3O+] |
| KH2PO4- |
= |
|
| |
|
[H2PO4- ] |
|
Třetí disociační konstanta pro
rovnici:
HPO4-2 + H2O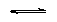 PO4-3 + H3O+ PO4-3 + H3O+ |
| |
|
[PO4-3].[H3O+] |
| KHPO4-2 |
= |
|
| |
|
[HPO4-2 ] |
|
Ovšem
platí, že
KH3PO4
(7,52.10-3)
> KH2PO4-
(6,23.10-8) >
KHPO4-2 (4,80.10-13), z tohoto
důvodu, lze zanedbat všechny disociační konstanty
vyjma první a s ní
počítat zcela obdobně jako v případě slabé jednosytné kyseliny |
| Takže uvažujeme, jak
výše uvedeno, pouze první disociační
konstantu : |
| |
|
[H2PO4-].[H3O+] |
| KH3PO4 |
= |
|
| |
|
[H3PO4 ] |
|
| Je zřejmé, že disociací vznikl stejný počet
molekul konjugované báze jako
oxoniových kationtů, to znamená,že se jejich
rovnovážné koncentrace rovnají: |
[H3O+] = [H2PO4-] |
| V disociační konstantě konjugovanou bázi nahradíme
oxoniovými kationty: |
| |
|
[H3O+].[H3O+] |
| KH3PO4 |
= |
|
| |
|
[H3PO4] |
|
| Rovnovážná
koncentrace
kyseliny [H3PO4] je menší (o disociované
molekuly, z každé z nich vznikl oxoniový kation) než
původní analytická koncentrace cH3PO4. ( řešení,
kde se toto zanedbává, je zde): |
[H3PO4]
= cH3PO4 -[H3O+] |
| Rovnovážnou koncentraci kyseliny nahradíme tedy koncentrací
analytickou
zmenšenou o koncentraci oxoniových kationtů:: |
| |
|
[H3O+].[H3O+] |
| KH3PO4 |
= |
|
| |
|
cH3PO4 -[H3O+] |
|
| Jedná se o kvadratickou rovnici: |
KH3PO4.cH3PO4 - KH3PO4.[H3O+]) = ([H3O+])2»»»
»»»([H3O+])2+ KH3PO4.[H3O+] - KH3PO4.cH3PO4= 0
| |
|
-KH3PO4
± {KH3PO42+4.KH3PO4.cH3PO4}1/2 |
| [H3O+] |
= |
|
| |
|
2 |
|
| Pro výpočty je toto vhodný výsledek, po výpočtu
[H3O+] se výsledek
zlogaritmuje, změní znaménko a získá se tak pH. |
pH = - log [H3O+] |
obecné
odvození,
výpočet, jednodušší
odvození
|