O B E C N
Ě
|
| Pro více - n-sytnou
kyselinu HnB platí n -
disociačních konstant |
První disociační konstanta pro
rovnici:
HnB + H2O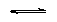 Hn-1B- + H3O+ Hn-1B- + H3O+ |
| |
|
[Hn-1B-].[H3O+] |
| KA1 |
= |
|
| |
|
[HnB ] |
|
Druhá disociační konstanta pro
rovnici:
Hn-1B- + H2O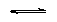 Hn-2B-2 + H3O+ Hn-2B-2 + H3O+ |
| |
|
[Hn-2B-2].[H3O+] |
| KA2 |
= |
|
| |
|
[Hn-1B- ] |
|
Až entá disociační
konstanta pro rovnici:
H1B-(n-1) + H2O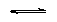 B-n + H3O+ B-n + H3O+ |
| |
|
[B-n].[H3O+] |
| KAn |
= |
|
| |
|
[H1B-(n-1) ] |
|
| Ovšem
platí, že KA1
> KA2
>.......>KAn-1>Kn (rozdíly ve
velikosti jsou velmi velké, několik řádů), z tohoto
důvodu, lze zanedbat všechny disociační konstanty
vyjma první a s ní
počítat zcela obdobně jako v případě slabé jednosytné kyseliny |
| Takže uvažujeme, jak
výše uvedeno, pouze první disociační
konstantu : |
| |
|
[Hn-1B-].[H3O+] |
| KA1 |
= |
|
| |
|
[HnB ] |
|
| Je zřejmé, že disociací vznikl stejný počet
molekul konjugované báze jako
oxoniových kationtů, to znamená,že se jejich
rovnovážné koncentrace rovnají: |
[H3O+] = [Hn-1B-] |
| V disociační konstantě konjugovanou bázi nahradíme
oxoniovými kationty: |
| |
|
[H3O+].[H3O+] |
| KA1 |
= |
|
| |
|
[HnB] |
|
| Rovnovážná
koncentrace
kyseliny [HnB] je menší ( o disociované
molekuly, z každé z nich vznikl oxoniový kation) než
původní analytická koncentrace cHnB. ( řešení, kde
se toto zanedbává, je zde): |
[HnB] = cHnB -[H3O+] |
| Rovnovážnou koncentraci kyseliny nahradíme tedy koncentrací
analytickou
zmenšenou o koncentraci oxoniových kationtů:: |
| |
|
[H3O+].[H3O+] |
| KA1 |
= |
|
| |
|
cHnB -[H3O+] |
|
| Jedná se o kvadratickou rovnici: |
KA1.cHnB - KA1.[H3O+]) = ([H3O+])2»»»»»»([H3O+])2+ KA1.[H3O+] - KA1.cHnB=
0
| |
|
-KA1±{KA12+4.KA1.cHnB}1/2 |
| [H3O+] |
= |
|
| |
|
2 |
|
| Pro výpočty je toto vhodný výsledek, po výpočtu
[H3O+] se výsledek
zlogaritmuje, změní znaménko a získá se tak pH. |
pH = - log [H3O+] |
konkrétní
odvození,
výpočet, zjednodušené
odvození
|