hydrazin
NH2NH2
|
| Pro dvousytnou
zásadu NH2NH2 platí 2 - disociační
konstanty |
První disociační konstanta pro
rovnici:
NH2NH2 + H2O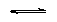 NH2NH3+ + OH- NH2NH3+ + OH- |
| |
|
[NH2NH3+].[OH-] |
| KNH2NH2 |
= |
|
| |
|
[NH2NH2 ] |
|
Druhá disociační konstanta pro
rovnici:
NH2NH3+ + H2O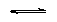 NH3NH3+2 + OH- NH3NH3+2 + OH- |
| |
|
[NH3NH3+2].[OH-] |
| KNH2NH3+ |
= |
|
| |
|
[NH2NH3+ ] |
|
| Ovšem
platí, že KNH2NH2
> KNH2NH3+ , z tohoto
důvodu lze zanedbat druhou disociační konstantu a
uvažovat pouze první a s ní
počítat zcela obdobně jako v případě slabé jednosytné zásady |
| Takže uvažujeme, jak
výše uvedeno, pouze první disociační
konstantu : |
| |
|
[NH2NH3+].[OH-] |
| KNH2NH2 |
= |
|
| |
|
[NH2NH2 ] |
|
| Je zřejmé, že disociací vznikl stejný počet
molekul konjugované kyseliny
jako hydroxidových aniontů, to znamená, že se jejich
rovnovážné koncentrace rovnají: |
[OH-] = [NH2NH3+] |
| V disociační konstantě konjugovanou kyselinu
nahradíme hydroxidovými anionty: |
| |
|
[OH-].[OH-] |
| KNH2NH2 |
= |
|
| |
|
[NH2NH2] |
|
| Jelikož pouze malé množství molekul zásady
přijímá vodíkové kationty, je rovnovážná koncentrace zásady [HB] jen o malinko menší (o ty
disociované molekuly) než původní analytická
koncentrace cHB. Při zanedbání tohoto
rozdílu, lze obě tyto koncentrace považovat za shodné
(zde klik na
řešení, kde se toto zjednodušení neprovádí): |
cNH2NH2 = [NH2NH2] |
| Rovnovážnou koncentraci zásady nahradíme tedy koncentrací
analytickou: |
| |
|
[OH-].[OH-] |
| KNH2NH2 |
= |
|
| |
|
cNH2NH2 |
|
| Nyní již můžeme vypočítat koncentraci
hydroxidových aniontů (analytickou koncentraci
totiž známe). |
[OH-] = (KNH2NH2.cNH2NH2)1/2 |
| Zlogaritmujeme: log[OH-] = 1/2(logKNH2NH2 + logcNH2NH2) |
| Obrátíme znaménka: -log[OH-] = 1/2(-logKNH2NH2
-
logcNH2NH2) |
| A zavedem p
parametry (pOH a pK): pOH
= 1/2(pKNH2NH2 - log cNH2NH2) |
| Převedeme na pH: pH= 14 -
pOH |
| pH = 14 - 1/2(pKNH2NH2
- log cNH2NH2) |
obecné
odvození,
výpočet, podrobné
odvození
|