Octan
amonný: CH3COONH4
|
| Ve vodě je disociován na: |
NH4+
a CH3COO- |
| Kation NH4+
v první reakci vystupuje jako kyselina: |
První
reakce:
NH4+
+ H2O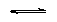 NH3
+ H3O+ NH3
+ H3O+ |
| Koncentraci iontů vzniklých disociací
vody jsme zanedbali |
| Některé
z H3O+ vzniklé v první reakci
vstupují do reakce s aniontem CH3COO-. |
Druhá reakce:
CH3COO- + H3O+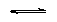 CH3COOH + H2O CH3COOH + H2O |
| Disociační
konstanta kyseliny CH3COOH (odpovídá druhé reakci zprava!!): |
| |
|
[CH3COO-].[H3O+] |
| KCH3COOH |
= |
|
| |
|
[CH3COOH] |
|
| Disociační
konstanta pro kyselinu NH4+ (odpovídá první reakci): |
| |
|
[NH3].[H3O+] |
| KNH4+ |
= |
|
| |
|
[NH4+] |
|
| Všechny sloučeniny v obou reakcích jsou ve stavu rovnovážném. Upozorňuji, že rovnovážná koncentrace H3O+
v obou reakcích je totožná. V první
reakci vzniklo H3O+
více, některé z H3O+ zanikly v reakci
druhé. |
[H3O+(rovnovážná)] =
= [H3O+(vzniklá)] - [H3O+(zaniklá)] |
| V první reakci vzniklo
NH3
stejně jako H3O+,
pro NH3 se zároveň jedná o koncentraci rovnovážnou,
neboť se v druhé reakci nevyskytuje a tudíž nemůže
ubývat jako [H3O+]. |
[H3O+(vzniklá)]=
= [NH3(vzniklá)] =
[NH3(rovnovážná)] |
| Disociační
konstantu kyseliny NH4+ lze tedy upravit: |
| |
|
[H3O+(vzniklá)].[H3O+(rovnovážná)] |
| KNH4+ |
= |
|
| |
|
[NH4+] |
|
| Z toho plyne, že koncentrace vzniklé
H3O+
je: |
| |
|
KNH4+.[NH4+] |
| [H3O+(vzniklá)] |
= |
|
| |
|
[H3O+(rovnovážná)] |
|
| V druhé reakci vznikala
CH3COOH
. Každá molekula CH3COOH
vznikla zánikem
H3O+,
znamená, že koncentrace vzniklé
CH3COOH
se rovná koncentraci zaniklé H3O+.CH3COOH
vzniklo tolik, až nastala její rovnovážná koncentrace: |
[CH3COOH
(vzniklá)]
=[H3O+(zaniklá)]
[CH3COOH
(vzniklá)]
= [CH3COOH(rovnovážná)]
[CH3COOH(rovnovážná)] = [H3O+(zaniklá)] |
| Disociační
konstantu kyseliny CH3COOH lze tedy upravit: |
| |
|
[CH3COO-].[H3O+(rovnovážná)] |
| KCH3COOH |
= |
|
| |
|
[H3O+(zaniklá)] |
|
| Z toho plyne, že koncentrace zaniklé
H3O+
je: |
| |
|
[CH3COO-].[H3O+(rovnovážná)] |
| [H3O+(zaniklá)] |
= |
|
| |
|
KCH3COOH |
|
| Pro rovnovážnou
koncentraci [H3O+] jak již výše
uvedeno platí: |
| [H3O+(rovnovážná)] =
[H3O+(vzniklá)] - [H3O+(zaniklá)] |
| Po dosazení pak: |
| |
|
KNH4+.[NH4+] |
|
[CH3COO-].[H3O+(rovnovážná)] |
| [H3O+(rovnovážná)] |
= |
|
- |
|
| |
|
[H3O+(rovnovážná)] |
|
KCH3COOH |
|
Po úpravě
platí:
[H3O+].[H3O+]. KCH3COOH = KNH4+.[NH4+].KCH3COOH
- [CH3COO-].[H3O+].[H3O+] |
| [H3O+].[H3O+]. ( KCH3COOH + [CH3COO-] ) = KNH4+.[NH4+] . KCH3COOH |
| [H3O+] |
= |
( |
| KNH4+.[NH4+].
KCH3COOH |
|
| KCH3COOH + [CH3COO-] |
|
) |
1/2 |
|
| Jelikož je disociační konstanta slabé
kyseliny KCH3COOH
mnohem menší , než
koncentrace [CH3COO-], můžeme
ve jmenovateli zanedbat KCH3COOH. |
| Jelikož se jedná o soli slabých kyselin a zásad,
můžeme jejich disociaci zanedbat a učinit rovny koncentrace
rovnovážné a analytické: |
[NH4+] = cNH4+
[CH3COO-] = cCH3COO- |
| Analytické koncentrace
cNH4+
a cCH3COO-
si musí (jsou totožné s analytickou
koncentrací jako celku, proto lze ve zlomku
krátit:: |
| [H3O+] |
= |
( |
KNH4+. cNH4+. KCH3COOH
|
|
cCH3COO- |
|
) |
1/2 |
|
[H3O+] =(KNH4+. KCH3COOH)1/2 |
| Po zlogaritmování : |
pH = 1/2 (pKNH4+ + pKCH3COOH) |
| Ovšem pK kyseliny NH4+
není tabelováno a proto využijeme vztahu
pro konjugovanou zásadu (viz. iontový
součin ): |
pKNH4+ + pKNH3 = 14»»»
»»» pKNH4+
=
14 - pKNH3 |
Takže výsledek:
pH
= 1/2 (14 - pKNH3 + pKCH3COOH) neboli:
| pH = 7 + 1/2 (pKCH3COOH - pKNH3) |
porovnej s výsledkem odvození var. B
!!! Výsledek není
závislý na koncentraci roztoku!!!
klik na obecné odvození , klik na příklad
|