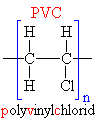
| Schématický
zápis: |
| n |
 |
|
 |
|
| Základní
pravidlo: |
| Platí zásada, že
sloučenina se "snaží" mít co nejmenší
náboj a pokud má existovat ion (ať už kation nebo
anion) "ochotněji" vznikne tam, kde je náboj
kompenzován částečným nábojem opačného znaménka,
neboli tam, kde je náboj v absolutní hodnotě menší
než jedna (Porovnej s
vlivem efektů u alkoholů u kyselin a u aminosloučenin).
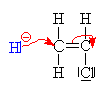
Proč je napadán mer
aniontem? Je to pro -
I efekt, který způsobuje
chlor pro svoji velkou elektronegativitu. Ten způsobí snížení elektronové
hustoty (částečně kladný náboj d+) na
uhlíku na nejž se váže . Z výše uvedeného plyne, že
více vadí a proto je snadněji napadnutelný uhlík, na
který se neváže chlor, neboť tam není náboj při
přesunu dvojné vazby ani částečně kompenzován.
Tento náboj je kladný a proto ho napadne anion. |
|
|
| Přehledný
podrobný zápis: |
| Iniciace: Hydrid
jako iniciátor (Lewisova
zásada) napadá
mer. |
|
|
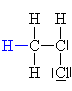
| Propagace: Po
napadnutí meru aniontem se vytvoří již objemnější
karboanion. Reakce pokračuje s dalším merem atd.
pořád dokola a karboanion se zvětšuje. |
|
|
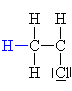
| Terminace:
Kation se napojí
na karbanion a výstavba makromolekuly se se tak ukončí(pozn.:
pro matemtické dogmatiky: počet merů v polymeru je tak
velký, že lze klást na roveň n a n+2 v dolním
vyčíslení). |
|
|
| zdepříklady:
obecně , s amidy , s alkalickými
kovy , s organokovy , s hydridy ). |