| Schématický zápis: |
| CH3CONH2 + C2H5OH |
| |
kat.H+ |
|
 |
| |
-NH3 |
|
|
CH3COOC2H5 |
|
| Podrobný zápis: |
| Esterifikace se děje v kyselém prostředí, to
znamená za přítomnosti silné minerální kyseliny (nejčastěji
kyselina
sírová)(porovnej s esterifikací v neutrálním prostředí ). Vodíkový kation jako elektrofilní
činidlo napadá p vazbu mezi
uhlíkem a vodíkem a v důsledku toho vzniká
karbokation s kladným nábojem na uhlíku (má ve třech
vazbách celkem 3 elektrony, jeden mu do čtyř chybí).
Na vzniklý karbokation se napojuje volný elektronový pár
kyslíku s hydroxoskupiny ethanolu (nebo, jestli chcete,
tak naopak, karbokation se jako elektrofilní činidlo
napojuje na volný elektronový pár na kyslíku). |
|
|
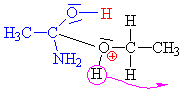
| V důsledku napojení vzniká kladný náboj na kyslíku
(má ve třech vazbách celkem 3 elektrony + 2 ve volném
elektronovém páru, jeden mu do šesti chybí), v
procesu obnovení 6 elektronů u kyslíku se odpojuje vodíkový
kation. |
|
|
| Vzniklý útvar je jako celek nestabilní a odštěpením
amoniaku přechází na ester. |
 |
|
| |
|
|
 |
| |
-NH3 |
|
|
| ethylester
kyseliny octové |
 |
|
|
|




![]()