| Další podmínkou
aromatického charakteru, vyplývající z dokonalé
konjugace, je planarita systému. |
| U aromatických
sloučenin vyjadřuje aromatický charakter jádro
znázorňované kruhem. Souběžně uváděné vzorce s
"dvojnými" vazbami jsou uváděny pouze pro
kontrolu počtu konjugovaných elektronů p.
Aromatické sloučeniny ve skutečnosti žádné dvojné
vazby nemají. |
| Benzen
C6H6
|
Nejznámější
aromatickou sloučeninou je benzen, Má 6
konjugovaných elektronů p. |
|
| Cyklopentadienylnatrium
C5H5Na
|
Další
aromatické sloučeniny se 6 konjugovanými
elektrony p jsou např. cyklopentadienylnatrium,
či cykloheptatrienyliumbromid (tropyliumbromid). |
Tropyliumbromid
C7H7Br
|
|
| Z kyseliny benzen-1-sulfonové
i z kyseliny benzen-2-sulfonové lze
další sulfonací připravit kyselinu benzen-1,6-disulfonovou
a kyselinu benzen-1,7-disulfonovou |
| Trifenylcyklopropenylium
perchlorát C3(C6H5)3ClO4
|
Trifenylcyklopropenylium
perchlorát - sloučenina s dvěma konjugovanými
elektrony p |
|
| |
| 1,3,5,7,9-cyklodekapentaen
C10H10
|
1,3,5,7,9-cyklodekapentaen
C10H10 by měl být
aromatickou sloučeninou, neboť má deset p elektronů. Sférické
interakce mezi "vnitřními vodíky jsou
značné a musí vést k deformaci molekuly. To
znamená, že je porušena konjugace p elektronů a tím
pádem sloučenina není aromatická. |
Cyklotriakontapentadekaen
C30H30
|
 Kurt
Mislow předpověděl
aromatický charakter až pro molekulu
cyklotriapentadekanu C30H30 s 30
konjugovanými elektrony p Kurt
Mislow předpověděl
aromatický charakter až pro molekulu
cyklotriapentadekanu C30H30 s 30
konjugovanými elektrony p |
|
|
| Hückelovo pravidlo
bylo odvozeno pro sloučeniny monocyklické, u
polycyklických uhlovodíků může vést v některých
případech k chybným závěrům. Přestože např. u
naftalenu či anthracenu "vyhovuje". |
| Naftalen 10 p el.
|
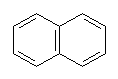 |
Anthracen 14 p el.
|
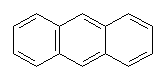 |
|
| Kliknutím
k pravidlům v organické chemii |

