
19.03.2005 20:34:32
[kliknutím k originálu
v angličtině][použit strojový překlad
eurotran]
John Frederic Daniell
narozen 12. března 1790, Londýn, UK
zemřel 13. března 1845, Londýn, UK
 |
John Frederic Daniell byl Britským chemikem a meteorologem, který vynalezl Daniellův článek, který byl velkým zlepšením oproti galvanické baterii používané v raných dobách vývoje baterie. |
John Frederic Daniell se narodil v Londýně, Anglie, 12 března
roku1790 jako syn právníka. On dostal dobré vzdělání, zatímco
chodí do soukromé školy. On prjímal jeden vydelal nebo cestný
titul od oxfordské univerzity.
 |
Na dokončení školy s dobrým pozadím v technice, chodil do práce pro príbuzného, který vlastnil cukrovar. Zatímco pracuje v rafinerii on zlepšil jeho technologické operace a procesy. Po awhile on nechal rafinerii zadat pole vzdělání a výzkum prijetím postoje jako profesor fyziky na univerzite Edinburghu, Skotsko, když jen 23 roku veku. V roce 1823, byl volen jako kolega v královské spolecnosti Londýna. Krome jeho tríd ve fyzice on také pracoval jako chemik na univerzite, a zacal výzkum meteorologie. Soubežný s jeho responsibilities univerzity on úspešne rídil kontinentální plynovou spolecnost v roce 1817. Daniell ne jen vynikal protože jeho schopnosti delat užitecné pozorování, klasifikace a zlepšení ve fyzikálních vedách jeho casu; ale on také projevil zrucnost pro vedecké výrobní podniky s vývojem nového procesu pro plyn generála. |
 |
Jeho výzkum v roce 1820 vedl k vynálezu vlhkomeru rosného bodu, který zmeril relativní vlhkost, která poté se stala standardním nástrojem. Jeho vlhkomer byl delán s dvema tenkými sklenenými žárovkami, které byly visel na základe a se spojoval se sklenenou trubkou. Jeden z žárovek skla držel éter a teplomer, který sbíral a rozptyloval rosu, když jiná žárovka byla pomalu chlazená a reheated. Kondenzacní teplota byla produkována odparováním éteru. Danielluv vlhkomer, jak to bylo voláno, umožnil snadné urcení páry to existovalo v daném množství atmosféry. Prumerná teplota zaznamenaná zarízením byla rosný bod. V roce 1823, on vydával Meteorologické eseje který brzy se stal oblíbenou knihou. Tato práce je “první pokus sbírat rozptýlené fakty na téma, a vysvetlit hlavní jevy atmosféry fyzikálními zákony. Daniell trval na nejvyšší duležitosti extrémní presnosti v meteorologickém pozorování, a vlastnil modelový dokument atmosferických zmen. On obrátil pozornost k nutnosti prijití k vlhkosti skleníku, a zpusobil revoluci ve vedení skleníku.” v pozdejším vydání on také diskutoval o meteorologických úcinkách slunecního zárení a tuhnutí Zeme. Danielluv esej o umelém klimatu zvažovaném v jeho použitích v zahradnictví ukázal význam vlhkosti v skleníkách. |
Zájem na atmosfére umožnil Daniella zlepšit skleníkovou rostlinu, která roste. On opravdu revolutionized horké domovní vedení tím, že zdurazní hodnotu vlhkosti ovzduší. Daniell byl první k užívacím fyzikálním zákonum ve zkoušení vysvetlit jev atmosféry. Jeho vedení práce k zlepšením ve vedení skleníku vyneslo jemu cenu stríbrné medaile od Horticultural spolecnost v roce 1824.
V roce 1830, on vynalezl pyrometer, který byl úspešný v merícím teple. Daniell shledal, že v kovech tavení kapalina je stále dojatá chlazením jeho zevnejšku. Jeho výzkum chemie umožnil jemu vyrábet plyn od pryskyrice a merit velmi vysoké teploty. On také vynalezl barometr vody v roce 1830.
Byl první profesor chemie a meteorologie na pak nové královské vysoké škole Londýna, a pracoval tam od 1831 k 1845. Zatímco na královské vysoké škole byl zodpovedný za založení oddelení aplikované vedy. V roce 1832, byl udelil Rumford medaili královské spolecnosti Londýna pro jeho casnejší práci s pyrometer.
Daniell, nicméne, je nejlépe známý
pro jeho práci v electrochemistry. Asimov prohlašuje,
že jeho zájem na výzkumu electrochemical byl povzbuzen jeho
prací prítel Faraday.
 |
 |
Pak v casném 1830s, Daniell stal se hluboce zaujatý v práci jeho prítele Michael Faraday tak se obrátil k electrochemistry pro jeho hlavní výzkumný zájem v té dobe. Hlavní problém s Volta hromadou byl že to nemohlo poskytovat proud udržovanému casovému období. Sturgeon pracoval na problému když v roce 1830 produkoval baterii s delším životem než to Volty tím, že sloucí zinek. Prispívání k hlavnímu problému s bateriemi bylo tenká vrstva bublin vodíku, které se tvorily pres pozitivní elektrodu. Tenká vrstva vodíku zpusobila zvýšený vnitrní odpor baterie, která redukovala jeho efektivní elektromotorickou sílu (napetí). Tento proces tenké vrstvy sbírání vodíku na elektrode je známý jako polarizace.
Daniell zacal experimenty v roce 1835 v pokusu zlepšit galvanickou baterii s jeho problémem bytí nestabilní a jako slabý zdroj elektrického proudu. Jeho experimenty brzy vedly k pozoruhodným výsledkum. V roce 1836, on vynalezl primární baterii ve kterém vodík byl vyrazen v generaci elektriny. Daniell rešil problém polarizace. V jeho laboratori on ucil se k slitine sloucený zinek jesetera se rtutí. Jeho verze byla první dva-tekutina trídit baterii a první baterii, která produkovala konstantní dobrý zdroj elektrického proudu pres dlouhé casové období. To je, síla zustala konstantní s tímto druhem baterie na opakované žádosti bez sejmutí kovy, které byly zdroj slabosti ve všech jednech tekutých bateriích. Do nynejška proud jiných baterií klesal rychle. Jeho umístení bariéry mezi medí a zinkové desky zabránili vodíku ve tvárení.
Volta baterie (hromada) vydávala volný vodík electrolyte
který pak se stehoval do pozitivní medené tyce. Vodík se
hromadil na tyci vytvorit prekážku to brzy zastavilo tok proudu.
Oba jediná tekutina a dva-baterie tekutiny používaly rešení,
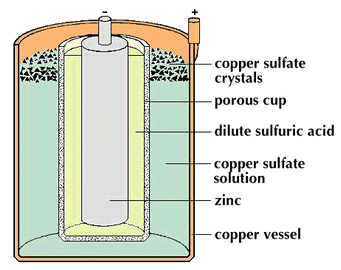
aby vytvoril elektrinu. Daniellova baterie sestávala z válcovité
medené lodi, která sloužila jako pasivní talír (tyc). Umístil
vnitrek vnejší medená lod byla porézní hlinená nádoba nebo
rozdelení, které drželo prut zinku nebo aktivní talír (tyc).
Prostor mezi medí a porézním pohárem byl naplnený rešením
z medi sulfát, který byl zustal naplnený krystaly lhaní soli
na derované polici. Porézní pohár byl naplnený zredenou
sulfuric kyselinou. Porézní hlinené zboží tajilo tekutiny
pred mixováním bez prekážení pruchod proudu; to dovolilo
iontum pohyb pres chvíli reakce bunky se konala. Obsahy baterie
musely být demontován když ne použitý zastavit chemické
reakce a zachovat kovy. Sulfát medi, která byla v spojení s
pasivním talírem posloužil, že zacne s vodíkem. Sloucený
zinkový prut (anoda) mela šroub vázání. Vrchol medeného válce
obsahoval jiné vázání prišroubovat (katodu).
 Schéma Daniellovy baterie - neodpovídá skutecné strukture toho. |
Chemická reakce uvnitr baterie sestávala z poklesu zinku a zvýšení z medi; zinek vytlacil med od jeho sulfátu tak že modrá skalice nepretržite se zmenila na sulfát zinku nahrazením. Beard a Rockwell vyjadroval chemickou reakci s rovnicí: Zn + H2Tak4
+ CuSO4 = |
 |
Kyselina sulfuric byla držena v porézním šálku predejít tomu od nepretržite jednat podle medi a zinku, a k živobytí sulfát zinku se tvoril od navázání med. Od modré skalice rešení je težké, to zustalo na dne bunky. Daniellova baterie s modifikacemi mela provozní napetí (tj. dal konstante elektromotorickou sílu a udržel témer konstantní vnitrní odpor) 1.11 volty. |
  |
Daniellovy nattery byly nazývány baterií konstanty, protože to nevypracovalo plyn, a proto nepolarizoval se, dodávat konstantní proud. To vybavilo jednotku elektrického potenciálu, volt jak sloupec rtuti delal jednotku odporu, ohm. Daniell bunka ješte používala známou med a elektrody zinku. Elektroda zinku byla dána v šálku unglazed hlinené zboží a namocený do zredené sulphuric kyseliny. Med byla obklopená krystaly modré skalice, která udržovala nasycený roztok. Místo toho, aby uvolnil vodík, elektrony byly zarízené k iontum medi v electrolyte, který pokrytý ven jako kov medi na nejakém blízkém povrchu. Úcel poháru mel udržovat se rešení se oddelí zatímco dovolí elektrické vedení stehováním iontu. Jestliže rešení se mísila, místní akce nicila baterii. Když bunka vybavila proud, zinek se rozpustil tvorit zinkové sulfátové rešení a med od modré skalice pokrytý ven na elektrode medi. |
Žádné plyny byly zahrnovány vubec, tak bunka se nepolarizovala. Bunka má docela velký vnitrní odpor, ale toto nebyla vážná porucha v pohledu na malé požadované proudy, a vlastne se ukázal jako výhoda v mnohých žádostech. To také chránilo bunku pred škodou jestliže shorted. Modrá skalice dokonce držela rasu pod kontrolou. Nicméne, porézní pohár, zamýšlený k živobytí rešení se oddelí, byl vyjádren odolný po case nánosem medi na tom jak bunka operovala.
Tento vnitrní odpor se menil mírne s oblastmi medi a zinkových
desek ponorených do rešení, vzdálenosti mezi plechy a šírky
a materiály zdí porézního poháru. Jeho provozní napetí záviselo
na hustotách medi a zinkových sulfátových rešení. Provozní
napetí se zvetšilo (napr., 1.14 V) zvýšením hustoty modré
skalice rešení a jeho napetí se snížili (napr., 1.08 V) tím,
že zvýší hustotu zinkového sulfátového rešení. Když
baterie nebyla v použití koroze zinkových desek byla vysoce
který velmi limitoval jeho dlouhovekost. Jeho baterie vyžadovala
malou údržbu, a nevydával škodlivé výpary. Daniell baterie
byla méne drahá než existující baterie. V roce 1837 (nebo
1836), on dostal Copley vyznamenání od královské spolecnosti
Londýna pro jeho práci s hromadou konstanty.
 |
Ilustrace ukazovat vnitrek venkovské telegrafní stanice s operátorem ženy. Zobrazení telegrafického vybavení je presné - na stolu operátora být smena telegraphicc, registr tisku, vypínac a camelback telegrafický klíc. Na podlaze skrín akumulátoru obsahuje dve Daniell bunky, který dodává elektrinu pro telegraf. |
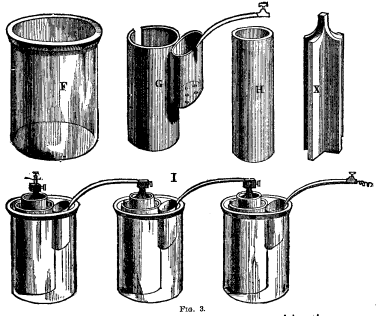 |
| Daniell baterie. Tato kombinace sestává ze džbánu skla nebo hlineného zboží, F (fík. 3), asi šest sune se v prumeru a osm nebo devet sune se vysoko. Talír medi, G, je ohnul do válcovité formy, aby hodil se uvnitr toho, a je vybavil s derovanou komorou, obsahovat zásobu sulfátu medi v krystalech a pás stejného kovu se svorkou pro spojování to k zinku príštího elementu. H je porézní pohár, jak to je technicky nazvaný, myslel si o unglazed hlinené zboží, šest nebo sedm sune se vysoko a dva sune se v prumeru, uvnitr který je umístil zinek, X. Toto je obvykle tvaru ukazovaného v císle, který je volán ` ` hrát zinek, ' ' ale to je casto vyrobeno ve forme dutého válce, druhého daní vetší moci ale bytí ponekud více obtížný uklízet. Vnejší bunka je naplnená nasyceným roztokem sulfátu medi (modrá skalice), a porézní bunka s rešením sulfátu zinku. Série trí elementu pripojila se spolu, jak obvykle upotrebil na amerických linkách pro místní baterii, je ukazován u Já. |
 |
Daniellova poslední práce na typu vážnosti baterie byla pozdeji se stát jedním nejpopulárnejší v roce 1850 . On se roztavil dva electrolytes; modrá skalice (CuSO4) a sulfát zinku (ZnSO4). Elektroda medi byla umístena ve spodní polovine sklenené bateriové sklenice a pak modrá skalice byla pridána v krystalové forme. Príšte zinkové sulfátové rešení bylo zatopeno nahore modré skalice. Tento prístup snížil potrebu pro porézní keramickou bránici se oddelit dva electrolytes, a omezil vnitrní odpor systému. Když obvod byl se otevrel a nechal chvíli postavení otevrený ionty medi by se šírily nahoru a self propuštení na anode zinku, která skoncila ztrátou moci. Operátor pridal krystaly modré skalice udržovat konstantní nasycený roztok, který pak mohl stále produkovat jeho proud. |
Danielluv výzkum vývoje bunek konstantního proudu se konal soucasne (pozdní 1830s) že komercní telegrafní systémy zacaly se objevit. Brzy zprávy telegrafu byly strucné a jely krátké vzdálenosti. Hrubé, slabé baterie byly dostatecné podporovat signál. Se zvyšováním provozu a zavedení Morsea soubory, silnejší proudy a více konstantní výstup byli požadovaní v bateriích. Daniellova med-baterie depolarized (1836) a Groveova dusicná kyselina depolarized bunka byla náhodné príjezdy. Britové a americké telegrafní systémy používali Daniell bunku výlucne, zatímco to byl ten jediný schopný bytí rychle depolarized. Jeho bunky také produkovaly konstantnejší výstup a tvorily silnejší proud než Sand baterie. Toto bylo “pre-volt” období, když intenzita bolesti byla používána jako míra síly bunky. Daniell bunka byla široce použitá ve Francii predtím Leclanché bunka byla vynalezena v roce 1868.
V roce 1839, Daniell experimentoval na fúzi kovu s 70-baterie bunky. On produkoval elektrický oblouk tak bohatý na ultrafialové paprsky že to skoncilo okamžitým, umelým úpalem. Tyto experimenty zpusobily vážné poškození ocí Daniella také jako oci diváku. Nakonec, Daniell ukazoval to iont kovu, ponekud než jeho kyslicník, nese elektrický náboj když kov-rešení soli je electrolyzed.
Daniell vydával úvod ke studiu filozofie chemikálie v roce 1839. V roce 1841, on se stal zakládajícím clenem a vicepresidentem chemické spolecnosti Londýna. On také napsal mnoho dokladu, které byly vydávány v žurnálech vedy.
Zatímco provádí výzkum v elektrolýze, kterou on opravil chyba na iontech delala dríve Faraday. On shledal, že kyseliny a základy nebyli ionty, a to jediné kovy nebo kov-jako separace a halogens a skupiny atomu separace kyseliny jsou ionty.
Daniell byl ilustrátor, sociální filozof, ucitel a spisovatel. Daniell se bral a byl otec peti dcer a dva synové. Zatímco jeden úcastnit se obecní schuze nebo mít prednášku u královské spolecnosti na 15 breznu 1845 on mel infarkt a umíral ve veku 55 let. U doby jeho smrti byl ministr zahranicí (1839-1845) královské spolecnosti.
![]() Tento text byl sestaven
z biografií of
Daniell available v internetu:
Tento text byl sestaven
z biografií of
Daniell available v internetu:
( 1,
2,
3, 4,
5,
6,
7,
8,
9,
10,
11
)