

27.03.2005 22:24:11
Fotografická
chemie
Fotochemické reakce jsou látkové
přeměny, probíhající působením světla. V přírodě jsou
velmi rozšířené. Jednou z nejdůležitějších fotochemických
reakcí je fotosyntéza. Patří sem však také například
blednutí barev nebo zrakový vjem, což je reakce světla s 11-cis-retinalem.
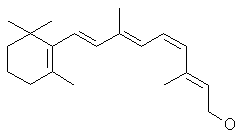
I když existuje mnoho látek,
které se účinkem světla mění, k fotografickému zobrazení
se užívá ve velkém jen jediná reakce – fotolytický
rozklad halogenidů (chloridu, bromidu nebo jodidu) stříbrných
na kovové stříbro a volné halogeny.
Ke vzniku obrazu bylo nejprve nutné neúnosně dlouhé ozařování slunečním světlem. Teprve roku 1839 zjistil Francouz L. J. M. Daguerre a nezávisle na něm Angličan W. H. Fox Talbot, že vrstvy chloridu nebo jodidu stříbrného stačí osvětlovat nepoměrně kratší dobu, jestliže se k získání výsledného obrazu použije dostatečné chemické zpracování (tzv. vyvolání). Nyní stačí pro vznik obrazu jen velmi krátká doba osvícení fotofilmu.
Základem vzniku obrazu je fyzikálně chemická změna halogenidu stříbrného (obsaženého v želatinové vrstvě fotofilmu), která se označuje jako vznik latentního (skrytého) obrazu. Redukce osvětlených halogenidů stříbrných se nazývá vyvolání. Převádění neosvětleného halogenidu na rozpustné sloučeniny se nazývá ustalování. Po jeho ukončení se získají trvalé, na světle stálé negativy nebo pozitivy.
Základem fotofilmů je světlocitlivá vrstva, tvořená želatinou, ve které jsou těžko rozpustné halogenidy stříbrné. V krystalu bromidu stříbrného je okolo každého kationtu Ag +1 šest aniontů Br.-1 a okolo každého aniontu Br.-1 – šest kationtů Ag+1 . Pokud jsou všechna místa v krystalové mřížce zaplněna, jsou náboje vyrovnány. Je – li však některá poloha neobsazená nebo obsazená cizím iontem, např. S.-2 , vzniká tzv. mřížková porucha. Taková místa mají zásadní vliv na citlivost fotografického materiálu.
Světelná energie působí na
krystal halogenidu stříbrného tak, že umožní odtržení
jednoho elektronu z bromidového aniontu:
Br -1
---světelná energie---› Br + e -1
Atom bromu buď reaguje
s jinou látkou (např. se želatinou citlivé vrstvy), nebo se
sloučí s jiným atomem bromu a vytvoří molekulu Br2
, která se vypaří do okolí:
2 Br -----›
Br2
V krystalové mřížce vzniká
přebytek elektronů. Ty se rychle slučují se stříbrnými
kationty, čímž vzniká atomární kovové stříbro:
Ag +1
+ e -----› Ag
Celý fotolytický rozklad
halogenidu stříbrného lze popsat rovnicí:
2 AgBr
-----› 2 Ag + Br2
Působí – li světlo na halogenid stříbrný dlouho, atomy stříbra se shlukují a můžeme pozorovat černání materiálu.
Podle toho, zda stříbro vzniklo ze stříbrných iontů, které byly přítomny v citlivé vrstvě u, nebo z iontů, které byly mimo citlivou vrstvu, dělíme vyvolání na fyzikální a chemické.
Fyzikální vyvolávání je proces, kdy se obraz tvoří ze stříbra, které se na fotomateriál ukládá z vývojky. Tohoto postupu se používá při zesilování fotografických obrazů. Základem je druhé vyvolání už ustáleného materiálu vývojkou, která obsahuje dusičnan stříbrný (AgNO3).
Větší význam má chemické vyvolávání. Při něm se obraz tvoří z exponovaného halogenidu stříbrného, přítomného v citlivé vrstvě. Na fotografický materiál se působí roztokem (tzv. vývojkou), jehož hlavní složkou je vyvolávací látka (viz výš). Kromě toho jsou v roztoku přítomny další látky, zajišťující stabilitu a správnou funkci vývojky. Je to např. látka, chránící vývojku před oxidací (např. siřičitan sodný Na2SO3) a dlaší látky (uhličitan sodný nebo draselný – K2CO3, hydroxid sodný nebo draselný, tetraboritan sodný – Na2B4O7, bromid draselný KBr aj.). Při vyvolávání dochází k redukci halogenidu stříbrného a současně k oxidaci vyvolávací látky (př.: vyvolávání hydrochinonem za vzniku 1,4 – benzochinonu)
Viditelný obraz se z obrazu latentního získává vyvoláním, což je redukce exponovaných stříbrných iontů vyvolávací látkou. Latentní obraz se při tomto procesu zesílí miliardkrát i více. Vyvolávací látkou nemůže být každá sloučenina, redukující halogenidy stříbrné. Musí to být takové redukční činidlo, které reaguje s exponovaným halogenidem podstatně rychleji než s neexponovaným. Jako vyvolávací látka se používá např.
 |
 |
 |
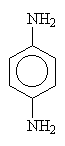 |
| p-fenylendiamin |
hydrochinon (1,4-dihydroxybenzen), pyrokatechol (1,2-dihydroxybenzen), p-fenylendiamin nebo pyrogallol (1,2,3-trihydroxybenzen). Všechny tyto látky jsou aromatické sloučeniny, především hydroxyderiváty nebo aminoderiváty benzenu. Substituenty (tedy aminoskupiny nebo hydroxyskupiny) musí být na benzenovém jádře nejméně dvě, a to v poloze ortho nebo para. Poloha meta je nevhodná pro podstatně obtížnější oxidaci fenolu, i když ani ta není zcela vyloučena, viz. poslední reakce v tabulce.Vzniklé vodíkové ionty (protony) se neutralizují zásadou, obsaženou ve vývojce.
|
||||||||||
|
||||||||||
|
||||||||||
|
||||||||||
|
Některá stříbrná zrna se vyvolávají úplně a některá vůbec. Rozdíly v optické hustotě částí fotografie tedy nejsou způsobeny tím, že by byly některé zárodky vyvolány více a jiné méně, ale různým počtem vyvolaných zárodků na jednotku plochy v různých místech fotografie.
Ustalování a vypírání. Vyvolaná citlivá vrstva ještě obsahuje na neexponovaných místech nezměněný halogenid stříbrný, který by působením světla černal a musí se proto stabilizovat. Tomuto procesu se říká ustalování. Provádí se působením roztoku thiosíranu S2O3 2 – . Thiosíran převádí nerozpustný halogenid na rozpustnou komplexní sloučeninu, která se pak odstraňuje vypíráním v čisté vodě.
AgBr + 2S2O3 -2 -----› [Ag (S2O3)2] -3 + Br -1
Ustálený materiál se musí důkladným vypírním zbavit veškerého thiosíranu stříbrného (Ag2S2O3; meziprodukt ustalování), jinak dochází k pozvolnému rozkladu působením kyslíku a vzdušné vlhkosti a stříbro v obrazu se mění na hnědý sulfid stříbrný Ag2S. Je – li třeba zajistit dokonalou trvanliost pozitivů, ponechávají se fotografické papíry před vypíráním asi na 3 minuty v roztoku uhličitanu sodného Na2CO3 ( = soda). Tím se doba vypírání zkrátí z 30 na 10 minut.
[fotochemie][chemická fyzika
a fyzikální chemi]
![]()